파이프라인
ONX-1006
ONX-1006 효능시험(예비)
AsPC-1 췌장암세포 이종이식모델에서 ONX-1006의 투여용량 설정시험, 2021년
| 시험군 | 투여액량(mg/kg) | PTX 용량(mg/kg) | |
|---|---|---|---|
| G1 | 음성대조군 | 0 | 0 |
| G2 | 시험물질 저용량 투여군 | 20 | 1.84 |
| G3 | 시험물질 중용량 투여군 | 50 | 4.6 |
| G4 | 시험물질 고용량 투여군 | 100 | 9.2 |
| G5 | Paclitaxel 투여군 | 20 | 20 |
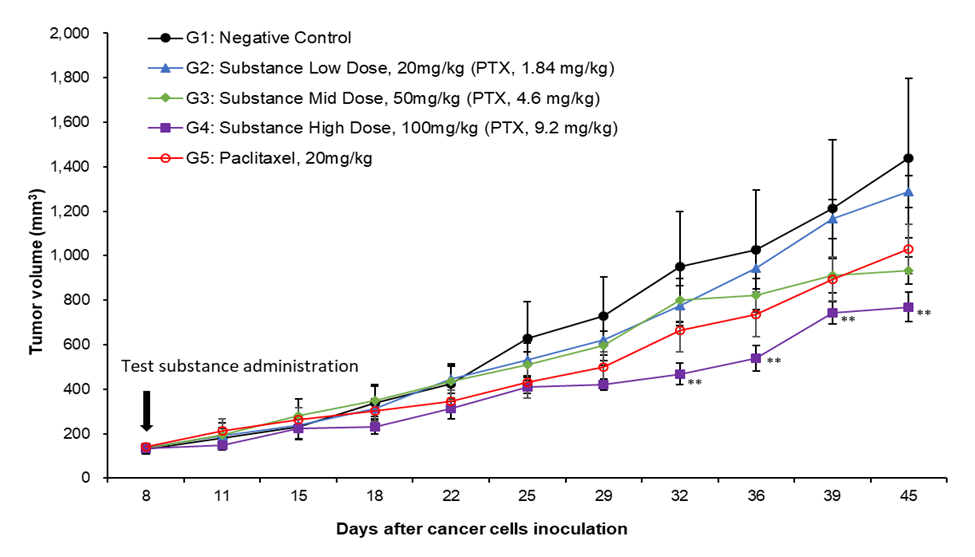
Figure 1. Tumor volume.
Test substance IV injection on Day 8, 15, 22, 29 and 36
Significant difference from the Negative control group by Dunnett's t-test: ** p < 0.01
Data presented mean ± S.E. (n=4)
테스트 기관 : 식품의약품안전처 인증사 ㈜디티앤씨알오.
테스트 결과 : 정맥 투여 방식으로 실시한 효능시험에서 획기적인 결과 및 효능입증( G3&G4 ).
→ 파클리탁셀 단독 투여량 대비 1/2 미만 ~ 1/4 의 용량 투여에도 훨씬 뛰어난 효능 입증
임상관찰에 유의한 영향 없음, 임상화학에 중대한 영향 없음, 체중 및Coagulation 변화 없음.
시험 후 ONX-1006 투여 동물들 전부 정상 상태로 부작용(독성) 없음이 확인됨.
ONX-1006 효능시험
ONX-1006 AsPC-1 췌장암 증식세포에 대한 효능시험, 2021년
| 시험군 | 투여액량(mg/kg) | PTX 용량(mg/kg) | |
|---|---|---|---|
| G1 | 음성대조군 | 0 | 0 |
| G2 | 시험물질투여군1 (저용량) | 68 | 10 |
| G5 | 시험물질투여군1 (저용량) | 68 | 10 |
| G7 | 아브락산 | 20 | 20 |
| G8 | 파클리탁셀 | 10 | 10 |

Figure 1. Tumor volume
Test substances were injected into mice (i.v) from 8th day after inoculation of AsPC-1 cell.
All data expressed mean ± S.E. (n=8).
Test substance IV injection on Day 8, 15, 22, 29, 36 and 42
테스트 기관 : 식품의약품안전처 인증사 ㈜디티앤씨알오.
테스트 결과 : 정맥 투여 방식으로 실시한 효능시험에서 획기적인 결과 및 효능입증( G2&G5 ).
→ 기존 항암제보다 진보된 아브락산( nab-paclitaxel )보다 뛰어난 항암효과 입증.
임상관찰에 유의한 영향 없음, 임상화학에 중대한 영향 없음, 체중 및Coagulation 변화 없음.
시험 후 ONX-1006 투여 동물들 전부 정상 상태로 부작용(독성) 없음이 확인됨.
ONX-1006: PANC-1 cell 췌장암세포 증식에 대한 효능시험 , 2020년

The results were statistically analyzed by ONE-WAY ANOVA * : Significantly different from G1 p<0.05 ** : Significantly different from G1 p<0.01 G1 : Vehicle control (n=9) G2 : Test article 1200 mg/kg (n=9) G3 : Test article 1900 mg/kg (n=9)
테스트 기관 : 식품의약품안전처 인증사 ㈜켐온
테스트 결과 : PANC-1 cell line 효능시험에서 통계학적으로 획기적인 결과 및 효능 입증
파클리탁셀 34mg/kg : (RAT 치사량) x 3 투여
파클리탁셀 54mg/kg : (RAT 치사량) x 5 투여
※ 파클리탁셀(PTX) RAT 치사량 : 10~12mg/kg
임상 관찰에 유의한 영향 없음, 임상 화학에 중대한 영향 없음, 체중 및 Coagulation 변화 없음.
ONX-1006 투여한 동물들 전부 정상인 상태로 확인됨 - 부작용(독성) 없음.
ONX-1006: MDA-MB-231 유방암 세포의 이종이식 마우스모델 효능시험 , 2021년

The results were statistically analyzed by Student’s t-test. * : Significantly different from G1, p<0.05 ** : Significantly different from G1, p<0.01 G1 : Vehicle control (Saline, n=10) G2 : Test article (ONX-1006, 100mg/kg, n=10) G3 : Test article (ONX-1006, 400mg/kg, n=10)
테스트 기관 : 식품의약품안전처 인증사 ㈜켐온
테스트 결과 : G3군 MDA-MB-231 cell line 효능시험에서 통계학적으로 획기적인 결과 및 효능 입증
임상 관찰에 유의한 결과 없음, 임상화학에 중대한 영향 없음, 체중 및 Coagulation 변화 없음.
ONX-1006 투여한 동물들 전부 정상인 상태로 확인됨 - 부작용(독성) 없음.

